他克莫司是一種強(qiáng)效免疫抑制劑,屬于大環(huán)內(nèi)酯類抗生素,從鏈霉菌屬中分離得到。它通過(guò)抑制鈣調(diào)磷酸酶的活性,阻止多種細(xì)胞因子生成,從而抑制T淋巴細(xì)胞的活化[1]。臨床上主要用于預(yù)防肝臟、腎臟等器官移植術(shù)后的移植物排斥反應(yīng),也可用于治療中重度特應(yīng)性皮炎[2]。此外,他克莫司還用于自身免疫性疾病如系統(tǒng)性紅斑狼瘡、膜性腎病等。

他克莫司是一種大環(huán)內(nèi)酯類強(qiáng)效免疫抑制劑,主要用于預(yù)防器官移植后的排斥反應(yīng),以及治療自身免疫性疾病,如系統(tǒng)性紅斑狼瘡、重癥肌無(wú)力等。然而,其臨床應(yīng)用面臨諸多挑戰(zhàn)[3]。首先,他克莫司治療窗窄,個(gè)體間藥代動(dòng)力學(xué)差異大,血藥濃度難以精準(zhǔn)控制,劑量不足可能導(dǎo)致排斥反應(yīng),而過(guò)量則增加不良反應(yīng)風(fēng)險(xiǎn)。其次,CYP3A5基因多態(tài)性顯著影響其代謝,不同基因型患者對(duì)藥物的代謝能力不同,進(jìn)一步增加了個(gè)體化用藥的復(fù)雜性[3]。此外,他克莫司的不良反應(yīng)較多,包括肝腎功能損害、高血壓、高血糖等,長(zhǎng)期使用還可能增加感染和腫瘤風(fēng)險(xiǎn)[4]。在臨床應(yīng)用中,不同疾病對(duì)藥物的療效和安全性要求各異,例如在狼瘡性腎炎和重癥肌無(wú)力治療中,其療效和安全性仍需進(jìn)一步驗(yàn)證。因此,他克莫司的臨床使用需要綜合考慮個(gè)體差異、基因檢測(cè)以及藥物監(jiān)測(cè)等多方面因素,以實(shí)現(xiàn)精準(zhǔn)用藥。
1.提高治療效果:
個(gè)體差異大:他克莫司在不同患者體內(nèi)的藥代動(dòng)力學(xué)存在顯著差異,相同劑量下,不同患者的血藥濃度可能相差很大。通過(guò)監(jiān)測(cè)血藥濃度,可以確保藥物達(dá)到有效的治療濃度,從而有效預(yù)防器官移植后的排異反應(yīng)。
治療窗窄:他克莫司的治療窗較窄,即最小有效濃度與最低中毒濃度接近。只有通過(guò)監(jiān)測(cè),才能將藥物濃度維持在合適的范圍內(nèi),確保療效。
2.預(yù)防藥物不良反應(yīng):
高濃度風(fēng)險(xiǎn):他克莫司的不良反應(yīng)與血藥濃度密切相關(guān),高濃度可能導(dǎo)致嚴(yán)重的不良反應(yīng),如腎毒性、神經(jīng)毒性等。通過(guò)監(jiān)測(cè)血藥濃度,可以及時(shí)發(fā)現(xiàn)藥物濃度過(guò)高的情況,從而調(diào)整劑量,減少不良反應(yīng)的發(fā)生。
個(gè)體化調(diào)整:不同患者的代謝速率不同,一些患者可能對(duì)藥物更敏感。監(jiān)測(cè)血藥濃度可以實(shí)現(xiàn)個(gè)體化用藥,避免因劑量不當(dāng)導(dǎo)致的不良反應(yīng)。
3.指導(dǎo)劑量調(diào)整:
動(dòng)態(tài)監(jiān)測(cè):他克莫司的血藥濃度受多種因素影響,包括患者的生理狀態(tài)、合并用藥等。通過(guò)定期監(jiān)測(cè),可以及時(shí)發(fā)現(xiàn)濃度變化,并根據(jù)監(jiān)測(cè)結(jié)果調(diào)整劑量,確保藥物濃度始終處于目標(biāo)范圍內(nèi)。
基因多態(tài)性:他克莫司的代謝受CYP3A5等基因多態(tài)性的影響,不同基因型患者的代謝速率不同。監(jiān)測(cè)血藥濃度可以幫助結(jié)合基因檢測(cè)結(jié)果,進(jìn)一步優(yōu)化個(gè)體化用藥方案。
4.優(yōu)化治療方案:
多因素綜合評(píng)估:在臨床實(shí)踐中,他克莫司的使用需要綜合考慮患者的臨床表現(xiàn)、血藥濃度、基因多態(tài)性等因素。通過(guò)監(jiān)測(cè)血藥濃度,結(jié)合其他臨床數(shù)據(jù),可以更全面地評(píng)估患者的治療反應(yīng),優(yōu)化治療方案。
長(zhǎng)期管理:對(duì)于器官移植患者,他克莫司的使用通常是長(zhǎng)期的。定期監(jiān)測(cè)血藥濃度有助于長(zhǎng)期管理患者的治療過(guò)程,及時(shí)發(fā)現(xiàn)潛在問(wèn)題,確保長(zhǎng)期治療的安全性和有效性。
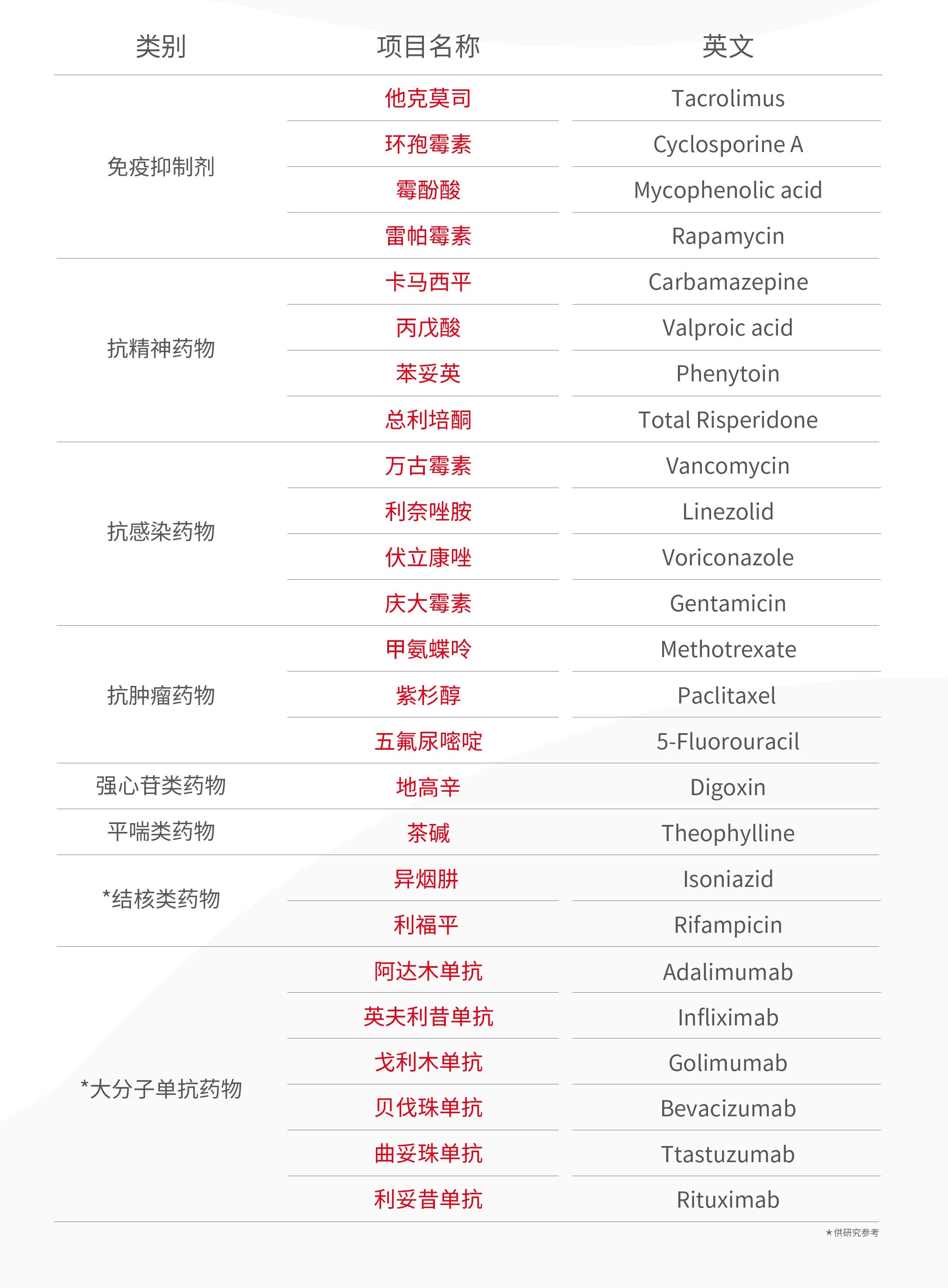
全自動(dòng)化學(xué)發(fā)光解決方案

參考文獻(xiàn)
1.Tang JT, Andrews LM, van Gelder T, et al. Pharmacogenetic aspects of the use of tacrolimus in renal transplantation: recent developments and ethnic considerations. Expert Opin Drug Metab Toxicol. 2016;12:555–565.
2.Christians U, Jacobsen W, Benet LZ, et al. Mechanisms of clinically relevant drug interactions associated with tacrolimus. Clin Pharmacokinet. 2002;41:813–851.
3.van Gelder T. Drug interactions with tacrolimus. Drug Saf. 2002;25:707–712.
4.de Jonge H, Naesens M, Kuypers DR. New insights into the pharmacokinetics and pharmacodynamics of the calcineurin inhibitors and mycophenolic acid: possible consequences for therapeutic drug monitoring in solid organ transplantation. Ther Drug Monit. 2009;31:416–435.